介入领域的发展趋势及血栓
介入治疗-是介于外科、内科治疗之间的治疗方法,在不开刀暴露病灶的情况下,在血管、皮肤上作直径几毫米的微小通道,或经人体原有的管道,在影像设备(DSA、透视机、CT、MR、B超)的引导下对病灶局部进行治疗的创伤最小的治疗方法。继传统药物治疗和外科开胸手术治疗后,介入治疗以其介入创伤小、手术危险小、疗效明显等优势开创了现代医疗的新领域。
随着遗传及环境作用的变化,血栓现已被公认为“沉默的杀手”,严重危害着人类的生命健康,与心肌梗死、脑卒中和静脉血栓栓塞症均密切相关。据“世界血栓日”专家委员会公布的数据显示每年全球范围血栓的发生接近1000万例,由血栓导致疾病而死亡的人数占总死亡人数的四分之一。
谱尼测试(300887)集团作为医疗器械领域的检测与验证的领军机构,有着丰富的介入产品检测的成功经验,助力众多医疗器械企业上市。今天与大家分享治疗血管狭窄或闭塞性病变的球囊扩张导管产品的风险等级管理类别、适用标准、注册单元划分等事宜。
产品结构及组成
球囊扩张导管一种头端带有可膨胀球囊的软性导管,用于在影像引导下扩张人体内狭窄的空腔脏器,如血管,消化道等通常由导管管体、球囊、不透射线标记、接头等结构组成,管体具有单腔或多腔结构,在靠近其末端处装有球囊。
作用机理及应用
球囊扩张导管是一种介入类医疗器械产品,球囊主要可以分为预扩张球囊、支架球囊和后扩球囊。首先,预扩张球囊到达病灶处,对血管进行预扩张处理。在血管预扩张处理完成之后,球囊导管承载支架进入血管,植入支架。完成支架植入后,后扩球囊进入血管,再次扩张,这可以使支架贴壁性更好,以减少患者形成支架内血栓的风险。球囊扩张导管在临床上主要应用于治疗血管狭窄或闭塞性病变。
产品风险等级
球囊扩张导管在我国《医疗器械分类目录》中,分类编码为03-13-06;管理类别为Ⅲ类。
注册单元划分
球囊扩张导管注册单元划分应重点考虑其产品的技术原理、结构组成、性能指标及临床预用途等因素,如:
◎ 冠脉球囊扩张导管、外周血管球囊扩张导管、神经血管球囊扩张导管宜分别划分为不同的注册单元。
◎ 整体交换型球囊扩张导管与快速交换型球囊扩张导管宜划分为不同的注册单元。
◎ 标称压力下球囊直径×球囊长度”相同但球囊制造材料不同的球囊扩张导管宜划分为不同的注册单元。
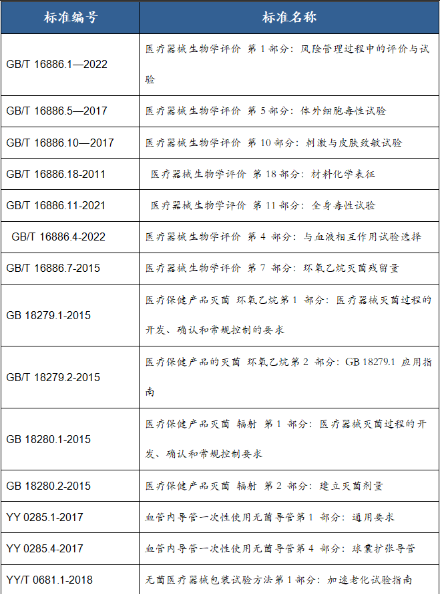
产品常用评价标准
谱尼医疗器械研发与评价全流程技术支持平台
谱尼测试集团在医疗器械检测领域具备CMA和CNAS资质,业务覆盖全国,我们竭力打造成医械产品快速上市的一站式高效服务平台,为医疗器械研发与临床前安全性评价提供全流程的技术支持,
业务范围涵盖:医疗器械材料的化学表征、理化检测、药物相容性检测和生物相容性检测、有源医疗器械的EMC电磁兼容实验、安规检测、无源医疗器械的理化性能检测、有机无机参数检测及生物、微生物性能检测。公司出具的检测报告均符合医疗器械国内注册、CE注册、FDA注册等法规要求,可为医疗器械企业提供从原料研发到最终产品验证与确认的全流程技术支持。
免责声明
本文来源为其他媒体的内容转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。